
digicomphoto / Getty Images
Ключевые выводы
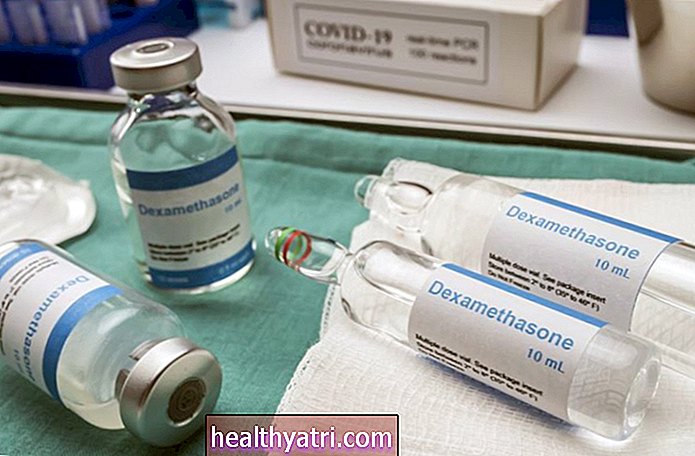
- Веклуры (ремдесивир) - первое одобренное FDA средство для лечения людей с COVID-19.
- Утверждение предназначено только для лечения госпитализированных пациентов с весом более 88 фунтов.
- Ранее препарат имел разрешение FDA на экстренное использование.
В четверг Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило препарат Веклуры (ремдесивир) для лечения COVID-19 у госпитализированных пациентов от 12 лет и старше. Это первый официально одобренный FDA препарат от COVID-19.
Ранее FDA выдавало ремдесивир Разрешение на использование в экстренных случаях (EUA), а не полное одобрение. В первом EUA, выпущенном 1 мая, говорилось, что ремдесивир можно использовать у госпитализированных пациентов с тяжелым COVID-19. EUA был переиздан 28 августа, и его использование было распространено на госпитализированных взрослых и детей с подтвержденными или подозреваемыми случаями COVID-19, независимо от тяжести их заболевания.
Хотя препарат сейчас одобрен, одобрение распространяется не на все группы. Для приема ремдесивира пациенты должны весить не менее 40 килограммов (кг) - около 88 фунтов. Стремясь и дальше предлагать этот препарат педиатрическим пациентам, подпадающим под действие первой EUA, при необходимости, FDA переиздалоеще одинEUA для использования ремдезивера в:
- Госпитализированные педиатрические пациенты с массой тела от 3,5 до 40 кг.
- Госпитализированные педиатрические пациенты младше 12 лет с массой тела не менее 3,5 кг.
«FDA стремится ускорить разработку и доступность средств лечения COVID-19 во время этой беспрецедентной чрезвычайной ситуации в области общественного здравоохранения», - сказал в своем заявлении комиссар FDA Стивен М. Хан, доктор медицины. «Сегодняшнее одобрение подтверждается данными нескольких клинических испытаний, которые агентство тщательно оценило и представляет собой важную научную веху в пандемии COVID-19. В рамках программы FDA по ускорению лечения коронавируса агентство будет продолжать помогать пациентам как можно скорее предлагать новые медицинские продукты, в то же время определяя, являются ли они эффективными и перевешивают ли их преимущества их риски ».
Что такое Ремдесивир?
Ремдесивир - это противовирусный препарат прямого действия, который подавляет синтез вирусной рибонуклеиновой кислоты (РНК). Коронавирусы, включая SARS-CoV-2, представляют собой семейство генома с одноцепочечной РНК. Было доказано, что ремдесивир останавливает репликацию этих вирусов.
Ремдесивир и COVID-19
Ремдесивир впервые попал в заголовки новостей весной, когда исследователи из Техаса определили внутривенное лекарство как «наиболее многообещающее средство лечения» COVID-19, несмотря на ограниченные клинические данные.
Когда появился SARS-CoV-2, исследователи увидели многообещающие результаты после тестирования ремдесивира на вирусе в лаборатории, и вскоре после этого начались клинические испытания, объясняет Мэтью Д. Холл, доктор философии, который работает в Национальном центре развития трансляционных наук при Национальном университете. Институты здоровья. Он помог создать портал COVID-19 OpenData Portal для обмена данными и экспериментами по перепрофилированию лекарств, связанных с COVID-19, для всех одобренных лекарств.
«На разработку большинства одобренных лекарств в среднем уходит 15 лет и пара миллиардов долларов, - говорит Холл Verywell. - Но у нас не было 15 лет; у нас не было даже 15 недель ".
Холл говорит, что ему и его команде было поручено оценить существующие ресурсы.
«Нам нужно было осмотреться, чтобы найти то, что уже было нам доступно и одобрено для лечения других болезней, или разрабатывались для лечения других болезней», - говорит он. «Возможно, они еще не одобрены, но, надеюсь, они были у людей, и мы знаем, что они безопасны. Нам повезло, что у нас есть много противовирусных препаратов. были наиболее активными, поэтому его можно очень быстро передать в клинические испытания ».
Мэтью Д. Холл, доктор философии
На разработку большинства одобренных лекарств уходит в среднем 15 лет и пара миллиардов долларов. Но у нас не было 15 лет; у нас не было даже 15 недель.
- Мэтью Д. Холл, доктор философииПервоначально FDA предоставило EUA 1 мая, чтобы разрешить госпитализированным взрослым пациентам с тяжелой формой COVID-19 лечить ремдесивиром. Человек с тяжелой формой COVID-19 был определен как:
- Пациент с сатурацией кислорода менее или равной 94%
- Пациент, которому требуется дополнительный кислород
- Пациент, которому требуется искусственная вентиляция легких
- Пациент, которому требуется экстракорпоральная мембранная оксигенация
Расширенный EUA помог сделать препарат доступным для пациентов на более ранних стадиях или с более легкими случаями заболевания, и одобрение должно только повысить его доступность. Холл говорит, что пациентам не нужно регистрироваться в рамках клинического обследования для получения лечения, что увеличивает доступ к людям, живущим в сельских общинах, которые не живут рядом с исследовательскими учреждениями.
«Я думаю, что все мы согласны с тем, что людям, которые просто немного нездоровы дома, было бы хорошо, если бы они приняли противовирусное средство, чтобы избавиться от вируса в своем организме раньше, чтобы они не заболели позже», - говорит Холл. «Прямо сейчас вам нужно подождать, пока вы не заболеете достаточно, чтобы лечь в больницу и получить ремдесивир. Было бы здорово убедиться, что эти люди никогда не заболеют настолько, чтобы пойти в больницу, дав им раньше противовирусное средство, такое как Тамифлю от гриппа, (когда) вы идете к врачу, получаете таблетку, и это сократит время, которое вам нужно заболели. "
Разработка Ремдесивира
Ремдесивир изначально был разработан в рамках сотрудничества между Gilead Sciences, Центрами по контролю и профилактике заболеваний США и Медицинским научно-исследовательским институтом инфекционных заболеваний армии США. Он изучался как потенциальное терапевтическое средство во время эпидемии вируса Эбола в Западной Африке и для двух других коронавирусов: тяжелого острого респираторного синдрома (SARS) и ближневосточного респираторного синдрома (MERS).
Кому следует принимать Ремдесивир?
Оптимальная популяция пациентов, дозировка и продолжительность лечения Ремдесивиром неизвестны. В информационном бюллетене для поставщиков медицинских услуг FDA предлагает следующие рекомендации:
- Для взрослых и детей с массой тела 40 кг и выше рекомендуемая доза составляет 200 мг в 1-й день с последующими дозами 100 мг.
- Для педиатрических пациентов с массой тела от 3,5 до 40 кг рекомендуемая доза составляет 5 мг / кг в день 1 с последующими дозами 2,5 мг / кг.
- Для пациентов, которым не требуется инвазивная механическая вентиляция и / или экстракорпоральная мембранная оксигенация, рекомендуемая общая продолжительность лечения составляет 5 дней.
- Для пациентов, которым требуется инвазивная механическая вентиляция и / или экстракорпоральная мембранная оксигенация, рекомендуемая общая продолжительность лечения составляет 10 дней.
- Если у пациента не наблюдается клинического улучшения, лечение может быть продлено до 5 дополнительных дней, а общая продолжительность лечения составляет до 10 дней.
Gilead Sciences работает над расширением производства и распространения ремдесивира, который считается исследуемым препаратом и в настоящее время не одобрен для каких-либо показаний.
Клинические испытания и предварительные выводы
Решение FDA одобрить ремдесивир основано на результатах нескольких клинических испытаний и вызвало неоднозначные мнения медицинского сообщества.
«То, что я думаю о любом наркотике или кандидате в наркотики, на самом деле не имеет значения, - говорит Холл. «Что действительно важно, так это данные хорошо контролируемого клинического исследования. FDA не расширило бы сферу действия EUA, если бы не считало, что это принесет пользу большему количеству пациентов ".
В исследовании, опубликованном 29 апреля вЛанцет,Группа врачей и исследователей провела рандомизированное двойное слепое плацебо-контролируемое исследование 237 взрослых пациентов с тяжелой формой COVID-19 в 10 больницах провинции Хубэй, Китай. Они обнаружили, что ремдесивир помогает ускорить выздоровление.
«Хотя это не является статистически значимым, пациенты, получавшие ремдесивир, имели численно более быстрое время до клинического улучшения, чем пациенты, получавшие плацебо, среди пациентов с продолжительностью симптомов 10 дней или меньше», - пишут авторы.
Исследование, спонсируемое правительством США, опубликовало свои предварительные результаты 22 мая вМедицинский журнал Новой Англиииз рандомизированного двойного слепого плацебо-контролируемого исследования 1063 пациентов с COVID-19. Исследователи обнаружили, что у тех, кому назначен 10-дневный курс ремдесивира, время восстановления было меньше по сравнению с плацебо - в среднем 11 дней по сравнению с 15 днями.
«Эти предварительные результаты подтверждают использование ремдесивира для пациентов, которые госпитализированы с COVID-19 и нуждаются в дополнительной кислородной терапии», - пишут авторы. «Однако, учитывая высокую смертность, несмотря на использование ремдесивира, очевидно, что лечение одним антивирусным препаратом вряд ли будет достаточным».
21 августаЖурнал Американской медицинской ассоциацииопубликовали рандомизированное исследование фазы 3 с участием 584 пациентов, госпитализированных с пневмонией COVID-19 средней степени тяжести. Производитель ремдесивира Gilead Sciences спонсировал это исследование в 105 больницах США, Европы и Азии. Пациенты получали 5-дневный или 10-дневный курс ремдесивира или получали стандартную помощь. Исследователи не обнаружили разницы в результатах среди 10-дневной группы и незначительной значимой разницы среди 5-дневной группы.
Все три исследования сталкивались с разными ограничениями и имели важные различия в дизайне, поэтому было бы несправедливо проводить сравнение яблок с яблоками. Тем не менее, это вызывает вопросы о повторении результатов, что является отличительной чертой клинических исследований.
«В настоящее время проводятся три [рандомизированных контрольных испытания] ремдесивира на госпитализированных пациентах с разными результатами, что поднимает вопрос о том, являются ли расхождения артефактами выбора дизайна исследования, включая популяцию пациентов, или препарат менее эффективен, чем предполагалось», - сказал Университет им. Исследователи Питтсбургской школы медицины написали в редакционной статье, опубликованной вЖурнал Американской медицинской ассоциации21 августа. «Поэтому представляется разумным срочно провести дальнейшие оценки ремдесивира в крупномасштабных рандомизированных контрольных испытаниях, направленных на устранение остаточных неопределенностей и информирование об оптимальном использовании».
Что это значит для вас
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США предоставило первое разрешение на лечение COVID-19 ремдесивиру. Если вы госпитализированы с подтвержденным или подозреваемым случаем COVID-19, ваш лечащий врач может принять решение о назначении этого препарата.
Что дальше с Ремдесивиром?
Согласно веб-сайту Gilead Sciences, в настоящее время проводятся дополнительные клинические испытания. Компания также находится на первой стадии разработки рецептуры ремдесивира в виде ингалятора.
Холл говорит, что мировое сообщество приняло вызов, но поиск лекарства от SARS-CoV-2 усугубляется тем фактом, что для лечения коронавирусов человека не существует терапевтических средств. Недавние вспышки SARS и MERS боролись с помощью мер общественного здравоохранения, а не лечения.
«Что касается ремдесивира, нам очень повезло, что он существует», - говорит Холл. «Нам повезло, что его разрабатывали для лечения лихорадки Эбола. Нам повезло, что сейчас он был доступен для испытаний на людях. Потому что, если вычесть ремдесивир из уравнения, я не знаю, что будет следующим лучшим вариантом. другой препарат, одобренный для лечения инфекции SARS-CoV-2 ».













-therapy-for-autism.jpg)





