Терапия, не зависящая от опухолей, относится к методам лечения рака, которые работают с разными типами рака. Другими словами, вместо того, чтобы работать только с одним типом рака, таким как рак груди, эти методы лечения могут работать для ряда различных видов рака, например, меланомы, рака груди и сарком. Кроме того, они могут работать как для взрослых, так и для детей.
Пануват Дангсунгнун / iStock
Вместо лечения, основанного на месте возникновения опухоли, эта терапия лечит рак, который возникает где угодно, в зависимости от определенных молекулярных характеристик, которые вызывают рост опухоли. Несмотря на то, что они возникают в разных тканях, очень разные типы рака нередко используют один и тот же путь для роста.
Более глубокое понимание биологии рака, возможность проводить геномное тестирование, чтобы определить, что является движущей силой роста конкретного рака, и доступность лекарств, нацеленных на эти пути, дали исследователям возможность лечить широкий спектр видов рака на молекулярном уровне. .
В настоящее время существует только несколько лекарств, одобренных специально для лечения опухолей, но ожидается, что в ближайшем будущем они будут быстро расширяться. Мы рассмотрим определение и важность методов лечения, не зависящих от опухоли, примеры, которые используются в настоящее время, а также преимущества и ограничения этого подхода к лечению.
Определение опухолевой агностической терапии
Терапия, не зависящая от опухоли, относится к использованию лекарств для лечения рака, основанных на молекулярном составе опухоли, а не на месте происхождения рака.
Важность
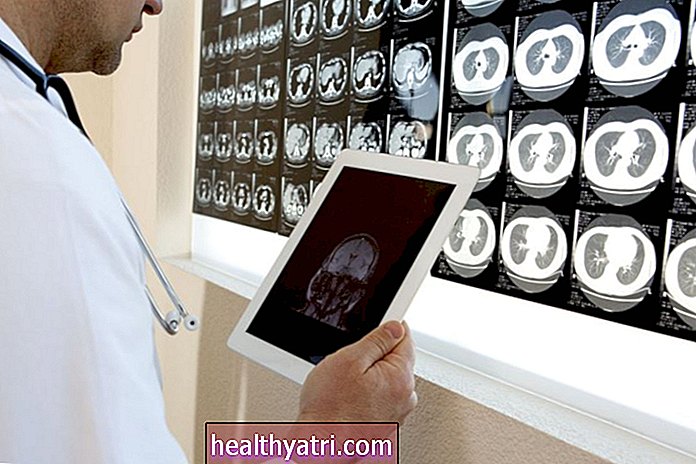
Лечение рака продвинулось настолько, что в отношении определенных типов рака (например, рака легких) методы лечения уже часто выбираются на основе молекулярных характеристик опухоли.
Например, при немелкоклеточном раке легкого вместо того, чтобы выбирать методы лечения, в первую очередь, на основе того, что видно под микроскопом, геномное тестирование (например, секвенирование следующего поколения) позволяет врачам определить, имеет ли рак конкретная генная мутация (или другое изменение). ), для которых теперь доступны таргетные методы лечения.
Хотя конкретный химиотерапевтический препарат можно назначать при нескольких типах рака, принцип лечения различен. Химиотерапия по существу лечит любые быстро делящиеся клетки.
Напротив, таргетная терапия (и, по-другому, иммунотерапевтические препараты) нацелена на очень специфический путь роста. Два рака одного типа и стадии, которые одинаково реагируют на химиотерапию, могут по-разному реагировать на лечение целевым препаратом.
Если опухоль несет в себе мутацию, такую как мутация EGFR, использование лекарственного средства, нацеленного на эту мутацию (например, ингибитора EGFR), с большой вероятностью приведет к контролю роста рака. Напротив, если опухоль не имеет этой мутации, маловероятно, что она вообще отреагирует на ингибитор EGFR.
Лечение, направленное на эти специфические геномные изменения (которые иногда называют «молекулярной сигнатурой» опухоли), значительно изменило как лечение многих видов рака, так и акцент на разработке лекарств.
Биология и терминология
Чтобы обсудить методы лечения, не зависящие от опухоли, полезно поговорить о некоторых запутанных биологических особенностях. К счастью, люди получают больше возможностей и узнают о своем раке, но это мало чем отличается от изучения сложного иностранного языка.
Чтобы рак продолжал расти, клетки должны достаточно отличаться от нормальных клеток, чтобы они не слушали нормальные сигналы организма, чтобы прекратить рост или уничтожить себя. В росте клеток задействованы сложные пути, и аномалии в некоторых из этих точек могут привести к неконтролируемому росту.
Генные мутации (и другие изменения) являются основой рака, и именно серия этих мутаций приводит к тому, что клетка становится раковой. Гены - это план для белков, а белки, в свою очередь, являются агентами, которые либо стимулируют, либо ингибируют различные точки этих путей.
В настоящее время существует ряд лекарств (и многие другие находятся в стадии разработки и клинических испытаний), которые ингибируют некоторые из этих белков и, следовательно, останавливают передачу сигналов, ведущих к продолжающемуся росту рака. Некоторые термины звучат очень запутанно, но при определении они довольно просты.
Термин «драйверная мутация» относится к мутации в гене, который кодирует белок, контролирующий рост рака. Рак с этой мутацией (или другим изменением) "зависит" от аномального белка, вырабатываемого для продолжения роста. Онкологи часто используют термин онкогенная зависимость для описания этого поведения.
Тогда конкретная мутация будет называться молекулярной сигнатурой рака.
Критерии противоопухолевого лечения
Чтобы лечение было эффективным при всех типах рака, необходимо соблюдать несколько критериев.
- Необходимо найти конкретную мутацию (или другое изменение). Другими словами, тестирование должно быть доступно для обнаружения изменений и выполняться довольно часто.
- Опухоли с определенной мутацией должны поддаваться лечению, нацеленному на лечение.
- Мутация должна быть обнаружена во многих различных типах рака.
Использование и примеры
В настоящее время существует несколько лекарств, одобренных для использования с независимыми от опухолей препаратами, а другие используются таким образом не по назначению. Мы рассмотрим некоторые из этих лекарств.
Кейтруда
Кейтруда (пембролизумаб) был первым лекарством, одобренным для лечения опухолевых агностиков в 2017 году. Кетруда - это PD-моноклональное антитело, классифицируемое как контрольный ингибитор (тип иммунотерапевтического препарата). реакция собственной иммунной системы организма на рак.
Кейтруда одобрена для лечения солидных опухолей у взрослых и детей с высокой микросателитной нестабильностью (MSI-H) или дефицитом репарации несоответствия (dMMR). Либо MSI-H, либо dMMR можно найти с помощью тестов, проводимых на опухоли (ПЦР или иммуногистохимия).
В 2020 году Кейтруда получила второе одобрение агностика опухолей для людей с солидными опухолями, которые имеют высокую нагрузку мутаций. Бремя мутаций является мерой количества мутаций, присутствующих в раковой опухоли, и связано (но не всегда) с положительным ответом на иммунотерапевтические препараты.
Витракви
Витракви (ларотректиниб) - второй препарат, который получил одобрение для лечения опухолевых агностиков в 2018 году. Он одобрен для взрослых и детей с опухолями с помощью слитых белков NTRK. Слияние гена нейротрофической рецепторной киназы (NTRK) встречается только примерно в 1% многих солидных опухолей, таких как рак легких, но может присутствовать до 60% некоторых типов сарком.
Некоторые из типов рака, на которые была продемонстрирована реакция, включают рак легких, меланому, опухоли GIST, рак толстой кишки, саркомы мягких тканей, опухоли слюнных желез, инфантильную фибросаркому, рак груди и рак поджелудочной железы.
У взрослых с опухолями, несущими слияние гена NTRK, частота ответа на Vitrakvi составляла от 75% до 80%, а в отдельном исследовании с участием детей общая частота ответа составила 90%.
Эти ответы наблюдались даже тогда, когда люди получали предыдущее лечение. Это подтверждает, насколько опухоли зависят от этого пути роста. Мало того, что отзывы были высокими, но и использование Vitrakvi позволило, выиграв несколько дел, позволить хирургам проводить менее уродливые операции на детях.
Розлитрек
В 2019 году FDA одобрило использование розлитрека (энтректиниба) для людей с опухолями, несущими слияние гена NTRK, а также при немелкоклеточном раке легкого с изменением ROS1.
Препарат был одобрен для взрослых и детей с метастатическим раком или для тех, у кого операция может привести к значительному обезображиванию. Во время оценки общий ответ редко составил 78%.
Наиболее распространенными видами рака в исследовании были саркома, немелкоклеточный рак легких, рак груди, колоректальный рак, рак щитовидной железы и секреторный рак аналога молочной железы.
Мутации BRAF
Хотя специфическая терапия, не зависящая от опухоли, не была одобрена, исследователи обнаружили, что люди с различными типами рака, несущими мутации BRAF, часто реагируют на лечение ингибиторами BRAF (обычно в сочетании с ингибитором MEK).
Мутации BRAF первоначально были отмечены (и лечились) у людей с метастатической меланомой, но теперь они были продемонстрированы при немелкоклеточном раке легкого (около 3%), раке толстой кишки, волосатоклеточном лейкозе, раке щитовидной железы, серозном раке яичников и других.
Другие примеры
Поскольку тестирование следующего поколения проводится все чаще, исследователи начинают видеть изменения генов, которые считались изолированными от одного типа рака в других типах.
Например, изменение, наблюдаемое при HER2-положительном раке молочной железы, присутствует у некоторых людей с раком легких.Другие примеры включают использование препарата Линпарза (олапариб) не только для лечения рака груди, но и рака яичников, рака простаты и рака поджелудочной железы, несущего мутацию BRCA.
Тестирование и испытания
В настоящее время ведутся разработки и клинические испытания ряда лекарств. Типы клинических испытаний, которые иногда оценивают лекарства для разных классов рака, включают корзины и зонтичные испытания. Оценка проводится с помощью протокола точного сопоставления NCI-MATCH.
Преимущества и ограничения
Когда дело доходит до возможности использовать одно лечение для нескольких различных типов рака, есть очевидные преимущества, но есть и ограничения.
Преимущества
Само собой разумеется, что препараты, не зависящие от опухолей, имеют преимущества, когда дело доходит до исследования и разработки лекарств. Разработка лекарств стоит очень дорого. Однако этот подход действительно выделяется при лечении редких видов рака.
С раком, поражающим лишь небольшой процент населения (например, детская фибросаркома), не обязательно «платить» компании за изучение и разработку лекарства. Нельзя сказать, что это неважно, но корпорации склонны вкладывать деньги таким образом, чтобы получить прибыль.
Однако при лечении опухолей, не зависящих от опухоли, фармацевтические компании могут получить компенсацию, если есть ряд людей с более распространенными формами рака, которым лекарство помогает. Пример - Витракви.
Еще одно сильное преимущество заключается в том, что исследования продвигают науку, касающуюся рака. Но, изучая молекулярные пути роста в надежде найти лечение, открываются новые пути с надеждой на еще большее количество методов лечения.
Ограничения / риски
Хотя методы лечения опухолевых агностиков могут показаться целью лечения будущего, их использование имеет ряд ограничений.
Не все виды рака реагируют одинаково
Даже когда два разных типа рака имеют одну и ту же мутацию, которая стимулирует рост рака, реакция на лекарство, нацеленное на эту мутацию, может быть очень разной.
Пример - мутации BRAF V600E. Меланомы или клетки лейкемии волосатых клеток, которые несут мутацию, как правило, очень чувствительны к лекарствам, ингибирующим BRAF. Напротив, рак толстой кишки с такой же мутацией не реагирует на ингибиторы BRAF.
Два типа рака, которые имеют одинаковую мутацию-драйвер, могут потребовать очень разных методов лечения для контроля роста.
Еще одно ограничение состоит в том, что геномное тестирование еще не стало рутинным для всех людей, даже с раком, при котором это настоятельно рекомендуется (например, при немелкоклеточном раке легкого). Для некоторых видов рака, особенно тех, которые наблюдаются нечасто, может быть мало данных об общих молекулярных характеристиках.
Чаще всего использование новых лекарств, особенно не зависимых от опухолей, доступно только в ходе клинических испытаний. Мало того, что участие в клинических испытаниях слишком низкое в Соединенных Штатах, но и существуют значительные различия в участии, которые затрудняют оценку лечения в зависимости от возраста, расы, пола и т. Д.
Развитие тоже требует времени. Согласно одному исследованию, среднее время от открытия лекарства до тестирования и утверждения в Соединенных Штатах составляет 15 лет. И даже когда эти методы лечения достигают продвинутого уровня в клинических испытаниях, они все равно могут помочь только меньшинству людей.
Наконец, цены на большинство новых методов лечения рака сейчас находятся в неустойчивом диапазоне.
Слово от Verywell
Лечение рака на основе молекулярных характеристик не ново, но использование этих методов лечения при многих типах рака можно рассматривать как прецизионную медицину на стероидах.
Несмотря на то, что происхождение рака (гистология) останется важным, начало фокусирования лечения на молекулярных характеристиках (геномика, иммунологические аномалии и т. Д.) Обещает продвинуть область онкологии такими способами, которые могут нас удивить не меньше, чем недавние достижения в области таргетной терапии и иммунотерапия.
В то же время приятно думать, что терапия, не зависящая от опухоли, может привести к лечению редких видов рака (особенно у детей), которые в противном случае были бы невозможны.