
Dex Images / Getty Images
Ключевые выводы
- FDA разрешило комбинацию бамланивимаба и этесевимаба для лечения COVID-19 у пациентов с высоким риском развития осложнений.
- Новая комбинация «значительно снизила» риск серьезных осложнений в клинических испытаниях.
- FDA ранее разрешило использовать только бамланивимаб.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) разрешило вторую терапию моноклональными антителами для лечения пациентов с COVID-19. Агентство выдало разрешение на экстренное использование (EUA) препаратов бамланивимаба и этесевимаба, используемых вместе для лечения COVID-19 легкой и средней степени тяжести у лиц в возрасте от 12 лет и старше, которые подвержены высокому риску развития тяжелой формы COVID-19.
Клиническое исследование показало, что однократная внутривенная инфузия бамланивимаба и этесевимаба «значительно снижает» риск госпитализации и смерти от COVID-19 в течение 29 дней наблюдения по сравнению с плацебо у пациентов с этим вирусом, которые подвергались высокому риску заражения. прогрессирующий до тяжелого заболевания.
В испытании участвовали 1035 не госпитализированных взрослых с легкими или умеренными симптомами COVID-19, которые имели высокий риск прогрессирования до тяжелой формы COVID-19, и давали им однократную инфузию 2800 миллиграммов бамланивимаба и этесевимаба или плацебо. Исследователи обнаружили, что 36 пациентов (7%), получавших плацебо, были госпитализированы или умерли, по сравнению с 11 (2%), которые лечились комбинированной терапией, что означает снижение на 70%. Было 10 смертей, и все были пациентами в группе плацебо.
FDA заявляет, что люди с «тяжелыми, длительными (хроническими) заболеваниями», такими как болезни сердца, болезни легких и диабет, «по-видимому, подвергаются более высокому риску госпитализации из-за COVID-19».
Это не первое лечение моноклональными антителами, разрешенное для использования FDA. Только в ноябре агентство выдало разрешение на регистрацию бамланивимаба.
Бамланивимаб «показал свою эффективность в снижении частоты госпитализаций среди пациентов с высоким риском прогрессирования заболевания, если его использовать на ранних стадиях заболевания», - сказал Сунанда Гаур, доктор медицинских наук, директор Центра клинических исследований в Медицинской школе Рутгерса Роберта Вуда Джонсона в Нью-Джерси. рассказывает Verywell.
Гаур говорит, что результаты испытания являются «многообещающими», но отмечает, что полные данные пока недоступны. Тем не менее, по ее словам, эта комбинация «потенциально более эффективна, чем один бамланивимаб».
Что это значит для вас
Когда разрешено другое лечение COVID-19, это всегда хорошие новости. Однако, если у вас нет основного заболевания, маловероятно, что это лечение будет доступно вам, если вы заразитесь COVID-19.
Как это работает?
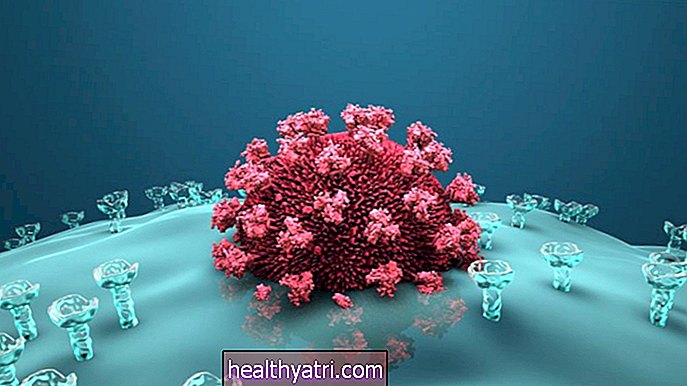
Бамланивимаб - это терапия моноклональными антителами, которая работает путем прямого связывания с частями вирусов, чтобы помочь им не заразить человека. Бамланивимаб нацелен на спайковый белок SARS-CoV-2, вируса, вызывающего COVID-19. Он разработан, чтобы блокировать способность вируса прикрепляться к человеческим клеткам и проникать в них. Лечение проводится через капельницу.
Этесевимаб также является моноклональным антителом, которое связывается с поверхностью рецептора белка шипа SARS-CoV-2. Этесевимаб работает аналогично бамланивимабу и был создан той же компанией Eli Lilly.
Не все подходят для этого лечения. FDA заявляет, что лечение могут проходить только люди в возрасте от 12 лет и старше, которые, как считается, имеют высокий риск серьезных осложнений, вызванных вирусом.
Бамланивимаб и этесевимаб не разрешены для пациентов, которые госпитализированы или нуждаются в кислородной терапии из-за COVID-19. Моноклональные антитела, такие как бамланивимаб и этесевимаб, могут вызывать худшие результаты у этих пациентов, особенно у тех, которым требуется высокий поток кислорода или механическая вентиляция.
Смешанные чувства
Хотя врачи приветствуют эту новость, некоторые отмечают, что многие специалисты в этой области не использовали моноклональные антитела. «Некоторые ждали дополнительных доказательств эффективности этих агентов в более крупных клинических испытаниях», - говорит Verywell Пратит Кулкарни, доктор медицины, доцент кафедры медицины инфекционных заболеваний Медицинского колледжа Бейлора в Техасе.
В результате «в медицинском сообществе отсутствует общая информация о моноклональных антителах», - говорит Verywell Ричард Уоткинс, доктор медицинских наук, врач-инфекционист и профессор внутренней медицины Северо-Восточного медицинского университета Огайо. И, добавляет он, «многие пациенты никогда о них не слышали».
Кулкарни отмечает, что последнее разрешение на использование в экстренных случаях основано на результатах более крупного клинического исследования фазы 3.
Само лечение также сложнее, чем просто прописать кому-нибудь таблетку, говорит Уоткинс, отмечая, что «существуют проблемы с персоналом с точки зрения проведения инфузий в амбулаторных условиях».
Гаур соглашается. «Это сложно с точки зрения логистики, так как требуется инфузия, которая может занять несколько часов», - говорит она. «Чтобы убедить врачей, потребуются более надежные данные о пользе такого подхода к раннему лечению».
Однако в целом Уоткинс считает разрешение многообещающим. «Я рад, что теперь у врачей будет еще один курс лечения для борьбы с COVID-19», - говорит он.





















.jpg)
