Поскольку количество случаев нового коронавируса (COVID-19) растет в результате прогнозируемого зимнего всплеска, в разработке находится ряд вакцин, которые помогут положить конец пандемии. Одна из них - вакцина Модерны, называемая мРНК-1273. Вакцина Moderna - вторая вакцина, получившая разрешение на использование в экстренных случаях от Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA).
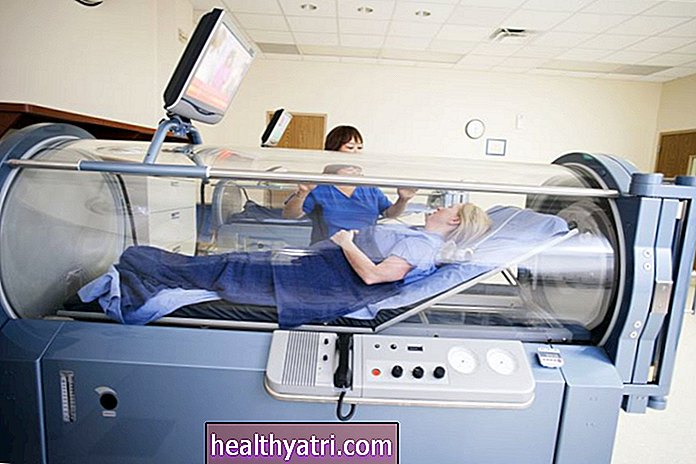
zoranm / Getty ImagesModerna, американская биотехнологическая компания, базирующаяся в Кембридже, штат Массачусетс, начала разработку своей вакцины в январе 2020 года. Компания работала с Национальными институтами здравоохранения (NIH) над завершением секвенирования генов вируса и вскоре после этого начала работу над разработкой вакцины.
Первая партия вакцины была разработана в начале февраля - всего через 25 дней после секвенирования гена. Первая доза вакцины была введена к марту 2020 года в рамках фазы 1 клинических испытаний, и эти первые испытания показали многообещающие результаты. К середине года Moderna получила финансирование и ускоренные регулирующие выплаты, чтобы способствовать развитию.
Хотя первоначально вакцина не ожидалась в течение 18 месяцев и более, новые разработки означали, что Moderna сможет доставить миллионы доз гораздо раньше. В августе 2020 года правительство США заказало 100 миллионов доз вакцины, хотя она еще даже не была одобрена для использования, а в ноябре были опубликованы результаты фазы 1 клинических испытаний.
В декабре были опубликованы результаты клинических испытаний фазы 3, и США заказали дополнительные 100 миллионов доз.
Когда была официально одобрена вакцина Moderna?
Американские чиновники здравоохранения предоставили вакцину Moderna разрешение на экстренное использование 18 декабря для взрослых в возрасте 18 лет и старше, что сделало ее второй вакциной, получившей обозначение от официальных органов здравоохранения США за одну неделю.
Как это устроено
Вакцина Moderna - это мРНК-вакцина, аналогичная вакцине, разработанной Pfizer. Технология, лежащая в основе этих вакцин, существует уже около трех десятилетий и оказалась многообещающей в предотвращении заведомо трудно поддающихся профилактике заболеваний - даже рака. В отличие от обычных вакцин, в которых используются инактивированные или живые вирусы, вакцины с мРНК неинфекционны и не содержат частей вируса, с которым они борются. Это делает вакцины на основе мРНК более безопасными для определенных групп населения.
Вакцина с мРНК (мессенджер рибонуклеиновой кислоты) представляет собой одноцепочечную молекулу, которая дополняет цепь вашей ДНК. Эти нити имеют специальное покрытие, которое может защитить мРНК от химических веществ в организме, которые могут ее разрушить, и помочь ей проникнуть в мышечные клетки.
Вместо того, чтобы подвергать организм воздействию небольшого количества вируса для создания иммунного ответа, мРНК заставляет реципиента вакцины производить интересующий белок. Это включает в себя:
- Помогая клетке сделать часть протеина с шипами, который делает COVID-19 таким мощным
- Обучение иммунных клеток распознаванию похожих белков с добавлением шипов и борьбе с ними
По данным Центров по контролю и профилактике заболеваний (CDC), вакцины с мРНК учат наши клетки, как производить белок - или даже просто кусок белка. Это вызывает иммунный ответ.
Вакцина Moderna первоначально была протестирована на взрослых в возрасте от 18 до 55 лет. В фазе 1 испытания были изучены три различных дозы - 25, 100 и 250 микрограмм - которые вводились дважды с интервалом в 28 дней. К фазе 3 исследования Moderna остановилась на двухдозовой формуле по 100 микрограмм каждая, вводимой двумя дозами с интервалом примерно в четыре недели.
Как была протестирована вакцина Moderna?
Фаза 3 исследования Moderna тестировала двухдозовую вакцину (по 100 микрограмм каждая с интервалом 28 дней) у взрослых в возрасте 18 лет и старше. В исследовании приняли участие более 30 000 участников, в том числе около 7500 взрослых в возрасте 65 лет и старше и более 5000 взрослых в возрасте от 18 до 64 лет с факторами риска тяжелого заболевания COVID-19.
Насколько это эффективно?
Исследователи, проводившие испытания, смогли проверить, насколько эффективна вакцина в создании антител и нейтрализации ответов с помощью тестов, в которых используются жидкости организма, такие как кровь или моча, чтобы увидеть, можно ли обнаружить антитела к определенному вирусу. Эти тесты включают:
- ИФА (иммуноферментный анализ) тест
- PsVNA (однократный анализ нейтрализации инфекции с репортерным псевдотипом лентивируса)
- PRNT (тест нейтрализации уменьшения зубного налета)
Уровни антител в этих тестах сравнивали с уровнями, обнаруженными у людей, вылечившихся от инфекции COVID-19. В исследовании изучались реакции других иммунных клеток, таких как Т-клетки.
После первого раунда вакцинации составами на 100 и 250 микрограмм в испытании фазы 1, ответы антител были аналогичны среднему уровню иммунитета у тех, кто выздоровел и имел естественный иммунитет после инфекции COVID-19.
Другие тесты на иммунитет, такие как PsVNA, показали слабый ответ после первой дозы. Однако после вторых доз антитела и другие иммунные ответы были сильными в группе вакцинированных, достигая уровней, которые были близки к уровням с наивысшими иммунными ответами у тех, кто выздоровел от COVID-19.
Согласно отчету об испытании, иммунный ответ развился примерно через две недели после первой дозы, но после второй дозы был намного сильнее.
Насколько это эффективно?
Вакцина Moderna оказалась очень эффективной - предотвращает COVID-19 у 94,1% людей, участвовавших в клинических испытаниях фазы 3. Кроме того, вакцина, по-видимому, обладает широкой эффективностью, причем показатели успеха одинаковы для разных возрастных, расовых, этнических и гендерных групп.
Срок службы этих вакцин еще не ясен, но руководители испытаний говорят, что они будут продолжать собирать образцы крови у исследуемой группы для проверки иммунитета в течение первого года после вакцинации. Как отмечается в отчете об испытаниях, в прошлом вирусы из одних и тех же семейств вирусов не вызывали долгоживущих иммунных ответов.
Когда это будет доступно?
Moderna получила разрешение FDA на экстренное использование вакцины 18 декабря.
Распространение может быть немного проще для Moderna, чем для Pfizer, поскольку вакцину можно хранить при стандартной температуре холодильника в течение 30 дней или замораживать при температуре около -20 градусов по Цельсию в течение шести месяцев. Вакцину Pfizer следует хранить при более низких температурах.
Что касается стоимости, Moderna объявила во время внутренней телефонной конференции в августе, что вакцина может стоить от 32 до 37 долларов за дозу, но окончательные цены могут измениться, когда пандемия пройдет.
Однако, по данным CDC, дозы вакцин, которые были закуплены правительством США, будут доступны гражданам бесплатно.
В дополнение к 200 миллионам доз, уже заказанным правительством США, у него есть возможность приобрести еще 300 миллионов.
По данным компании, по состоянию на 26 января Moderna поставила в США 30,4 миллиона доз, из которых 10,1 были введены. Moderna также объявила, что планирует доставить в США 100 миллионов доз к концу марта и еще 100 миллионов доз к концу июня.
Компания также достигла соглашений о поставках вакцины в несколько других стран, в том числе:
- Европейский Союз: 80 миллионов начальных доз с возможностью еще 80 миллионов доз
- Япония: 50 миллионов доз
- Канада: 40 миллионов доз с возможностью еще 16 миллионов.
- Швейцария: 7,5 миллиона доз
- Великобритания: 7 миллионов доз
- Израиль: 6 миллионов доз
По данным Moderna, ряд других стран также разместили заказы компании, но количество заказанных доз не разглашается.
Хотя сама вакцина будет бесплатной, если будет закуплена государством, поставщики вакцины, которые вводят вакцину, могут взимать плату. Программы возмещения этих административных расходов должны быть доступны как через государственные, так и частные планы страхования, а также через Фонд помощи поставщикам Управления ресурсов и услуг здравоохранения для людей, не имеющих государственного или частного медицинского страхования.
Вакцины от COVID-19: будьте в курсе того, какие вакцины доступны, кто может их получить и насколько они безопасны.
Кто может получить вакцину Moderna?
Теперь, когда вакцины разрабатываются, возникает вопрос, кто их получит и когда? CDC ожидал ограниченных поставок на начальном этапе программы вакцинации, и рекомендации относительно того, кто должен получить вакцину в первую очередь, были сделаны Консультативным комитетом CDC по практике иммунизации (ACIP) в декабре 2020 года на основе более ранних рекомендаций Национальной академии наук, инженерии. , и медицина.
Что касается приказа, федеральные чиновники здравоохранения решили, что медицинские работники и люди, живущие в учреждениях долгосрочного ухода, должны первыми получить первые вакцины, которые поначалу были ограничены по мере наращивания производства.
По данным CDC, в США более 18 миллионов поставщиков медицинских услуг и около 1,3 миллиона американцев живут в учреждениях долгосрочного ухода. Каждому из этих людей нужно будет получить две дозы основных претендентов на вакцину, что в сумме составит около 40 миллионов доз, необходимых для начальной фазы вакцинации. По оценкам CDC, потребуется несколько месяцев, прежде чем предложение вакцин удовлетворит спрос.
Рекомендации относительно того, кто получит вакцину и когда, будут решены по мере поступления запасов. Только в США проживает около 330 миллионов человек, а это означает, что для вакцинации всей Америки потребуется около 700 миллионов доз вакцины, поскольку другие вакцины следуют за двумя дозами вакцины.
Хотя информации о том, когда и где вакцинацию будут проходить, пока мало, государственные и местные департаменты здравоохранения будут координировать усилия по распределению доз вакцины по мере их поступления. Вакцина должна быть доступна как в кабинетах врача, так и в местах розничной торговли, например, в аптеках, где вводятся другие вакцины.
Вакцина Moderna вводится двумя дозами с интервалом 28 дней. CDC рекомендует вводить вторую дозу как можно ближе к 28 дням, но предоставляет четырехдневный льготный период, когда ее можно вводить немного раньше, и позволяет в некоторых случаях вводить вторую дозу в течение 42 дней после первой дозы. где 28-дневное окно невозможно.
Когда дети смогут получить вакцину?
Дети сначала не будут получать вакцину, поскольку испытания проводились только на взрослых. Moderna начала набор участников для клинического исследования среди детей в возрасте от 12 до 17 лет в декабре. Испытания для детей младшего возраста все еще находятся на стадии планирования. Дети и подростки могут получить вакцину позже в 2021 году.
Побочные эффекты и нежелательные явления
Людей, принимавших участие в исследовании, просили записывать любые реакции на вакцину, будь то область, в которую вводилась вакцина, или общая реакция. Боль в месте введения вакцины и общая усталость были наиболее частыми побочными эффектами в испытании фазы 3.
Системные эффекты - это реакции, которые влияют на все тело, а головная боль и усталость возглавляют этот список и были наиболее частыми в группе вакцинированных. Менее 20% вакцинированных людей сообщают о повышении температуры тела после второй дозы.
С другой стороны, локальные эффекты влияют только на небольшую ограниченную область. Наиболее частым эффектом в этой категории была боль в месте укола.
При приеме второй дозы вакцины выраженность реакций увеличивалась. Немногие реакции были оценены как тяжелые после первой дозы вакцины, но некоторые были оценены как тяжелые после второй дозы. Наиболее частыми реакциями, о которых сообщили участники после второй дозы вакцины, были:
- Боль в месте укола
- Усталость
- Головная боль
- Мышечные боли
- Озноб
- Боли в суставах
Также сообщалось о тошноте или рвоте, лихорадке, покраснении или опухших участках в месте инъекции, а также опухших или увеличенных лимфатических узлах.
Процент серьезных побочных реакций был одинаковым для групп плацебо и вакцины (0,6%) и не указывал на какие-либо проблемы с безопасностью. В испытаниях также не было доказательств ассоциированного с вакциной усиленного респираторного заболевания. Предыдущие вакцины против коронавируса в ветеринарии и на моделях животных приводили к респираторным проблемам, связанным с вакцинацией.
Со временем будет проводиться больше наблюдений за учебными группами, и планируется больше исследований на особых группах населения, например, на детях.
Финансирование и развитие
Moderna работала с Национальными институтами здравоохранения и Министерством здравоохранения и социальных служб США над разработкой вакцины. Компания получила около 1,6 миллиарда долларов федерального финансирования через Управление передовых биомедицинских исследований и разработок (BARDA) - правительственную программу США, направленную на ускорение производства и распространения вакцин для борьбы с COVID-19. Правительство США воспользовалось своим правом на еще 100 миллионов доз от Moderna примерно на 1,68 миллиарда долларов.





.jpg)